Всё возрастающее загрязнение водных объектов вызывает тревогу во всех странах мира. Ежегодно в поверхностные водные объекты сбрасываются миллионы кубометров загрязнённых сточных вод, содержащих самые разнообразные загрязняющие вещества, что в значительной мере ухудшают качество поверхностных вод [1].
Так, например, многие водные объекты Белгородской области не соответствуют нормативным требованиям по различным показателям [1].
Для очистки промышленных и бытовых сточных вод используют различные способы, методы и приёмы [3]. В последнее время исследователи всё чаще обращают внимание на промышленные отходы, которые, благодаря своим физико-химическим и механическим свойствам могут быть использованы для очистки сточных вод [2].
К одним из таких отходов относится пыль электрофильтров предприятий по производству железобетонных изделий (ЖБИ) ООО "ЖБИ-4" г. Белгород. В ходе технологических процессов: (погрузка, выгрузка, транспортировка, дозирование, пересыпка, перемешивание), образуются пылегазовые выбросы. Пыль, улавливаемая системой пылегазоочистки, в настоящее время не используется, а складируется на полигоне промышленных отходов.
В результате исследований нами было установлено, что в состав пыли входят такие соединения как: хатрурит Ca3SiO5, ангидрит Ca(SiO4), браунмиллерит Ca2(Al,Fe+3)2O5, ларнит Ca2SiO4, гроссит CaAl4O7, гипс CaSO4(H2O)2, альбит NaAlSi3O8.
При добавлении пыли к водной среде происходит увеличение значения pH (рис.1),которое возрастает в интервале концентраций пыли от 0 до 3 г/дм3, достигая значения 12.0, а затем кривая роста PH выходит на плато.
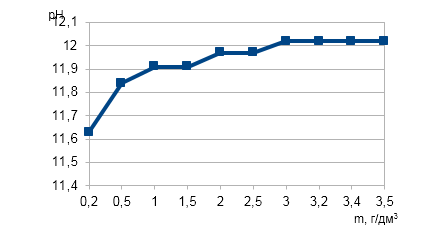 Рис.1. Зависимость pH воды от массы добавки пыли электрофильтров
Рис.1. Зависимость pH воды от массы добавки пыли электрофильтров
На рис.2 видно, что достижение значения pH=12 происходит в первые 5 минут наблюдения, а затем стабилизируется на уровне pH=12. Таким образом, для максимального подщелачивания среды достаточна добавка пыли массой 3 г/дм3 и длительность перемешивания 5 минут. (Рис.2)
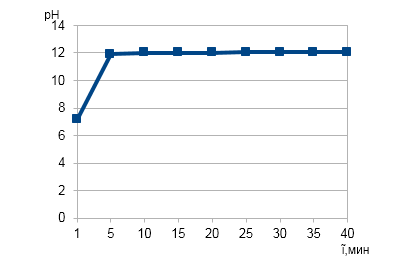 Рис. 2. Зависимость pH воды от времени контакта
Рис. 2. Зависимость pH воды от времени контакта
Возрастание значения pH создаёт благоприятные условия для образования малорастворимых гидроксидов металлов, которые легко удаляются из раствора фильтрованием или отстаиванием [2].
Для того, чтобы определить достаточное количество добавляемой пыли, при котором достигается максимальная степень очистки, проводились исследования зависимости эффективности очистки от массы добавляемой пыли электрофильтров. В серии опытов использовались модельные растворы, содержащие ионы Ni2+с концентрацией 10 и 20 мг/дм3. (рис.3)
К 100 мл модельного раствора добавляли расчётное количество пыли электрофильтров. Масса навески составляла от 0,3 до 1,2 г/дм3 раствора. Длительность перемешивания составляла 10 минут во всех опытах. После перемешивания суспензию фильтровали через бумажный фильтр, в фильтрате определяли концентрацию ионов Ni2+ на фотоэлектроколориметре (ФЭК) при установленной длине волны. λ=490 Н*м.
Эффективность очистки рассчитывали по формуле:
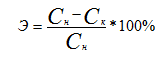 ,
,
где Сн – начальная концентрация, мг/дм3;
Ск – конечная концентрация, мг/дм3.
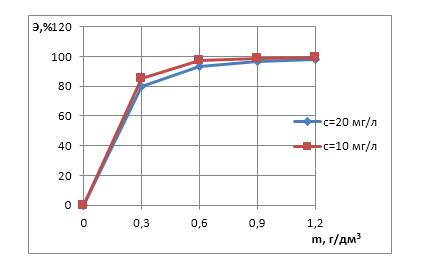
Рис.3. Зависимость эффективности очистки модельных растворов, содержащих ионыNi2+ от массы добавки пыли электрофильтров
(100 мл р-ра; 10 мин; t = 20°C)
Как видно из рис.3, оптимальная навеска пыли электрофильтров, при которой наблюдается максимальная степень очистки (96.6%), составляет 0,9 г/дм3.
Таким образом, в работе установлена принципиальная возможность использования пыли электрофильтров для извлечения ионов Ni2+ из растворов.
Научный руководитель:
Свергузова Светлана Васильевна, доктор технических наук, профессор, зав. кафедрой «Промышленная экология» Белгородского государственного технологического университета им. В.Г. Шухова, г. Белгород, Россия

 Е.
А. Беловодский
Е.
А. Беловодский