Аннотация. Статья посвященаактуальной проблеме – умягчение жесткости воды. Целью является разработка недорогой синтетической смолы из отечественного сырья. В рамках сформулированной цели на данный момент проведены следующие виды работ: улучшена технология процесса синтеза смолы для умягчения жесткости грунтовых вод; подобраны оптимальные условия синтеза полимера; выработана экспериментальная партия смолы; по итогам апробации смолы на ООО «Городской Оздоровительный Комплекс» г. Стерлитамак был получен «Акт о внедрении результатов научного исследования», который подтверждает положительный эффект синтезированного вещества в умягчении грунтовых вод в котельных ООО «Городской Оздоровительный Комплекс». Проанализировав все известные методы и классификации ионообменных смол, нами на основе стирола и акриловой кислоты, а также стирола, малеинового ангидрида и акриловой кислоты в присутствии инициатора получены синтетические смолы, которые могут использоваться для умягчения, обессоливания и очистки воды в котельных, водозаборных станциях, ТЭЦ и т.д. Полученные синтетические полимеры обеспечивают как лучшую очистку воды за счет адсорбции ионных примесей на поверхности ионообменной смолы, так и эксплуатационные свойства смолы, и полную их регенерацию после работы.
Ключевые слова: ионообменные смолы, водоподготовка, радикальная полимеризация, инициатор - порофор, стирол, ацетон, малеиновый ангидрид, акриловая кислота, диоксан, бензол, снятие кинетики, титрометрический метод анализа, трилон Б.
В настоящее время в промышленном производстве стоит острая проблема умягчение жесткости воды. Использование жёсткой воды вызывает появление осадка (накипи) на стенках котлов и трубах. В энергетике случайное кратковременное попадание жесткой воды в систему очень быстро выводит из строя теплообменное оборудование, трубопроводы, поэтому жесткость воды для теплообменного оборудования ограничена очень малыми значениями 0,02-0,03 ммоль - экв/л [1, c. 110].
Одной из основных задач в технологии водообработки является выбор оптимальных видов реагентов, определение условий их применения и необходимых доз. В технологии умягчения воды широко применяют ионообменные смолы, которые представляют собой специально синтезированные полимерные нерастворимые в воде вещества, содержащие в своей структуре ионогенные группы кислотного характера –SO3Na [2, c. 247].
Ионообменные смолы в основном классифицируют на катионообменные и анионообменные смолы.
Среди сильнокислотных катионообменников отечественного производства, разрешенных к применению для очистки воды можно выделить КУ-2–8чС. Получают его сульфированием сополимера стирола с 8% - ным раствором дивинилбензола. Недостатком этого катионита является сильная набухаемость при cмачивании, в результате чего меняется его молекулярная структура, а также он обладает небольшой динамической обменной емкостью около 1,6 г - экв/л [4].
Среди сильноосновных анионитов широкое применение нашли марки АВ-17-8, предназначенные для водоподготовки, гидрометаллургии, очистки сточных и возвратных вод, а также для химической промышленности, однако стоит отметить, что аниониты в процессе эксплуатации стареют вследствие окисления кислородом, растворенным в воде. Это приводит к снижению обменной емкости анионита. Для регенерации анионитов расходуется большое количество щелочи по сравнению со стехиометрически необходимым (до 20 кг NaОН на 1 кг удаляемой кремнекислоты), что доказывает не эффективность этого метода. [3, с. 152].
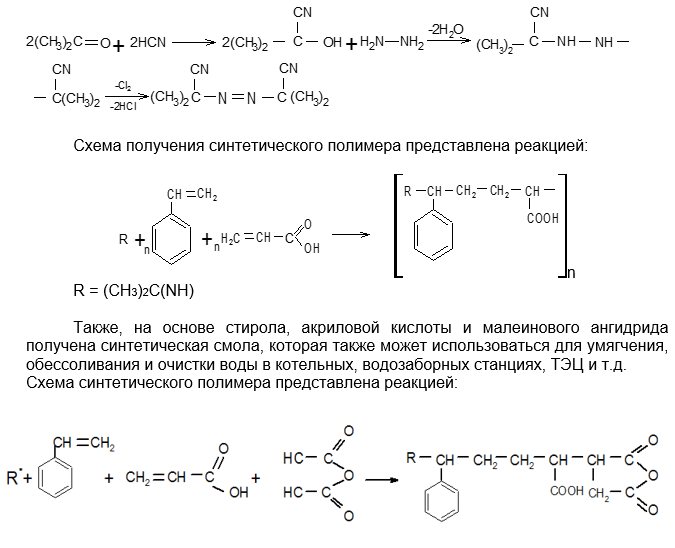
Проанализировав вышеперечисленные методы и классификации ионообменных смол, нами на основе стирола и акриловой кислоты получена синтетическая смола, которая может использоваться для умягчения, обессоливания и очистки воды в котельных, водозаборных станциях, ТЭЦ и т.д. Реакция идет под действием инициатора 2,2’ – азоизобутиронитрил (порофор N).
Азонитрилы получаются конденсацией кетона с синильной кислотой, а затем с гидрозином (в виде сульфата) и последующим окислением образующегося производного гидразина хлорной водой [4, с. 572].
Экспериментальная часть.
Методика получения высокомолекулярной синтетической ионообменной смолы.
В трехгорлую колбу, снабженную механической мешалкой, термометром, обратным холодильником и водяной баней, загружали 26 г стирола,18 г акриловой кислоты, 0,5 г порофора, в качестве растворителя использовали 200 г бензола. Реакционную смесь интенсивно перемешиваем при температуре бани 94 °С и температуры смеси 84 °С в течении 2 ч, затем отбирали пробу на содержание кислоты в смеси, которую титровали 0,1 н. NaOH. Смесь перемешивали в течении 4 ч при температуре смеси 84°С. Соотношение стирола и акриловой кислоты к бензолу 4:1. Полученную смесь омылили в 40% растворе щелочи, полученные при этом продукты представляют собой сополимеры, содержащие в своем составе функциональные группы -COONa. Полученный полимер высадили в соляной кислоте, полимер выпал в осадок.
Методика получения низкомолекулярной ионообменной смолы.
В трехгорлую колбу, снабженную механической мешалкой, термометром, обратным холодильником и водяной баней, загружали 26 г стирола,18 г акриловой кислоты, 0,5 г порофора, в качестве растворителя использовали 222 г ацетона. Реакционную смесь интенсивно перемешивали при температуре бани 65 °С и температуры смеси 61 °С в течении 2 ч, затем отбирали пробу на содержание кислоты в смеси, которую титровали 0,1 н. NaOH в присутствии индикатора фенолфталеина. Соотношение стирола и акриловой кислоты к ацетону 4:1. Полученную смесь омылили в 60% растворе щелочи. Полученные при этом продукты представляют собой сополимеры, содержащие в своем составе функциональные группы -COONa. Полученный полимер высадили в соляной кислоте, полимер выпал в осадок.
В процессе работы полимер получился низкомолекулярным, т.к. очень хорошо растворился в щелочи. Полимер отфильтровали от кислоты, промыли водой, высушили. Полимер получился в виде порошка желтого цвета.
Методика получения ионообменной смолы.
В трехгорлую колбу снабженную механической мешалкой, термометром, обратным холодильником и электрической плиткой, загружали 26 г стирола,18 г акриловой кислоты, 24,5 г малеинового ангидрида, 0,5 г порофора, в качестве растворителя использовали 274 г диоксана. Реакционную смесь интенсивно перемешивали при температуре смеси 102 °С в течении 4 ч, затем отбирали пробу на содержание кислоты в смеси, которую титровали 0,1 н. NaOH в присутствии индикатора фенолфталеина. Соотношение исходных веществ к диоксану 4:1. Полученную смесь омылили в 1% растворе щелочи. Полученные при этом продукты представляют собой сополимеры, содержащие в своем составе функциональные группы -COONa. Полученный полимер высадили в воде, полимер выпал в виде белых комков.
В сводной таблице 1 указаны исходные реагенты, растворители и температуры их кипения.
Таблица 1
Исходные реагенты, применяемые растворители и температуры кипения смесей
|
№ опыта |
Исходные реагенты |
Растворитель |
Температура кипения смеси, °С |
|
1 |
акриловая кислота, стирол, порофор |
ацетон |
61 |
|
2 |
акриловая кислота, стирол, порофор |
бензол |
84 |
|
3 |
акриловая кислота, стирол, малеиновый ангидрид, порофор |
диоксан |
102 |
В качестве примера титраметрическим методом мы проанализировали жесткость грунтовых вод, использовавшихся в котельных ООО «Городской оздоровительный комплекс»:
Исходя из экспериментальных данных, мы видим, что при использовании синтезированного полимера жесткость воды составляет 0,25 ммоль – экв/л, что подтверждает эффективность работы полученного полимера.
Полученная ионообменная смола имеет ряд преимуществ по сравнению с общепринятыми смолами для водоумягчения. Она может применяться как для умягчения воды промышленного, так и для бытового применения, а также по сравнению с известными смолами она наименее дорогостоящая, так как в основу получения полимера входит акриловая кислота, которая не является дефицитом в нашем регионе в связи со строительством акрилового завода в г. Салават.
Ссылки на источники
- Акользин, П. А. Коррозия и защита металла теплоэнергетического оборудования. – М.: Энергоиздат, 1984. – 304 с.
- Ваюцкий, С. С. Курс коллоидной химии. – М.: Химия, 1975. – 513 с.
- Неницеску, К. Д Органическая химия. – М.: Химия, 1963. – 863 с.
- Комарова Л.Ф., Кормина Л. А. Инженерные методы защиты окружающей среды. – Барнаул: Алтай, 2000. – 254 с.
- http://www.ekomarket.ru/info/softwater

 А.
А. Тихонова
А.
А. Тихонова